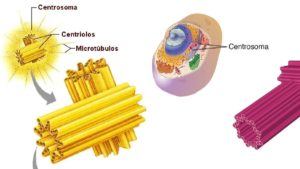
Los bioelementos son las unidades que componen los seres vivos y se unen para formar diferentes biomoléculas . Las biomoléculas son de lo que están hechos los seres vivos.
Los seres vivos, como toda la materia del universo, están formados por partículas muy pequeñas llamadas átomos. Estas partículas son tan pequeñas que no se pueden ver con un microscopio. Los átomos son el primer nivel estructural de la materia y están organizados en moléculas. Sabemos que hay 117 tipos diferentes de átomos. Cada uno de estos forma un elemento químico. Un elemento químico es una forma de materia que consta de un tipo de átomo.
Los bioelementos son elementos químicos que se convierten en parte de las biomoléculas o que, de alguna manera, intervienen en las funciones de la materia viva. Conozcamos ahora mejor qué son los Bioelementos y biomoléculas: estructura y funciones.

Los diversos elementos químicos que precisa una especie para desarrollarse con normalidad, se llaman bioelementos. Tenemos los cuatro primarios que son, el nitrógeno, el hidrógeno, el carbono y el oxígeno. Después tenemos el fósforo y el azufre.
Clasificación de los bioelementos

Según el papel que desempeñan en los sistemas biológicos, los bioelementos se pueden clasificar en bioelementos del grupo I, II y III.
Bioelementos primarios
Éstos representan un 96.2% de la totalidad. O, C, H, N, P, S. Son los elementos químicos como el carbono, el hidrógeno, el nitrógeno, el azufre y el fósforo que forman parte de los compuestos orgánicos de las biomoléculas y que son responsables de sus características funcionales.
Bioelementos secundarios
Su proporción es menor que los primarios, pero igual de importantes. En un medio mojado están siempre ionizados, Na⁺, K⁺, Ca²⁺, Mg²⁺, CI¯.
Estos son los elementos químicos activos principalmente como iones de metales alcalinos o alcalinotérreos. Se encuentran principalmente disueltos en líquidos biológicos.
A veces forman sales insolubles que forman materiales esqueléticos (vertebrados) o conchas (moluscos).
Oligoelementos o del grupo III
Estos bioelementos se encuentran en seres vivos en menos de un 0.1%. Algunos de ellos están presentes en todos los seres vivos (bioelementos indispensables), y los otros solo se encuentran en ciertos organismos (los variables). Es un grupo además que suele estar formado por metales de transición (manganeso, zinc, hierro, cromo, cobalto, cobre, molibdeno, níquel). Estos elementos químicos realizan importantes funciones catalíticas.
Además de los elementos mencionados anteriormente en la clasificación anterior, hay elementos como el silicio (que forma las capas de las diatomeas) que son difíciles de catalogar pero que probablemente tienen una función secundaria.
Los elementos químicos que más abundan en la corteza y en los seres:
- Los compuestos son fácilmente diluyentes en el agua, con lo que permite fácilmente su incorporación y su eliminación.
- El C y N tienen la misma similitud para unirse al hidrógeno o al oxígeno, con lo que pasan con la misma capacidad de un estado oxidado al estado reducido. Estos procesos de oxidación-reducción son el principio de casi todos los procesos químicos importantes, sobre todo de los que se relacionan con la adquisición de energía como los son la fotosíntesis o la respiración celular.
- El C, H, O, y N son los elementos de una mínima parte atómica y tienen variabilidad de valencias, con que pueden realizar enlaces covalentes entre sí. Después de esto, se crean muchas variedades de moléculas de enorme tamaño. De todos ellos, el más importante es el carbono. Éste es un átomo es una base para la química orgánica y la de los seres vivos.
Las biomoléculas

A partir de los bioelementos, podemos decir, se forman las biomoléculas, que son esas sustancias químicas particulares cruciales para el buen funcionamiento de los seres vivos.
Ejemplos de biomoléculas, de hecho, son lípidos, vitaminas, carbohidratos, fosfatos, hormonas y neurotransmisores que, esencialmente compuestos de carbono e hidrógeno (bioelementos), realizan una gran lista de tareas.
Además del carbono y el hidrógeno, las biomoléculas a menudo contienen otros elementos, como oxígeno, nitrógeno, fósforo y azufre, mientras que hay menos hierro y magnesio.
En definitiva, las biomoléculas son los bioelementos unidos entre sí formando moléculas que componen a los seres vivos. Éstas se clasifican en diferentes principios inmediatos, cuyo nombre se debe a la facilidad con la que extrae la materia viva a través de métodos simples como la evaporación, filtración, disolución.
Enlaces químicos de los bioelementos

La forma en que los elementos interactúan entre sí depende de cómo están dispuestos sus electrones y cuántas aberturas para electrones existen en la región más externa donde los electrones están presentes en un átomo. Los electrones existen a niveles de energía que forman capas alrededor del núcleo. La capa más cercana puede contener hasta dos electrones. La capa más cercana al núcleo siempre se llena primero, antes de que se pueda llenar cualquier otra capa. El hidrógeno tiene un electrón; por lo tanto, solo tiene un lugar ocupado dentro del caparazón más bajo. El helio tiene dos electrones; por lo tanto, puede llenar completamente la capa más baja con sus dos electrones.
Si observas la tabla periódica, verás que el hidrógeno y el helio son los únicos dos elementos en la primera fila. Esto se debe a que solo tienen electrones en su primera capa.
Aquí tienes la tabla periódica:
El segundo y tercer nivel de energía pueden contener hasta ocho electrones. Los ocho electrones están dispuestos en cuatro pares y una posición en cada par se llena con un electrón antes de completar cualquier par.
Al mirar nuevamente la tabla periódica, notarás que hay siete filas. Estas filas corresponden al número de celdas que tienen los elementos dentro de esa fila. Los elementos dentro de una fila particular tienen un número creciente de electrones a medida que las columnas avanzan de izquierda a derecha. Aunque cada elemento tiene el mismo número de capas, no todas las capas están completamente llenas de electrones. Si observas la segunda fila de la tabla periódica, encontrará litio (Li), berilio (Be), boro (B), carbono (C), nitrógeno (N), oxígeno (O), flúor (F), y neón (Ne). Todos estos tienen electrones que ocupan solo las capas primera y segunda. El litio tiene solo un electrón en su capa más externa, el berilio tiene dos electrones, el boro tiene tres, y así sucesivamente, hasta que la capa completa se llena con ocho electrones, como es el caso del neón.
No todos los elementos tienen suficientes electrones para llenar sus capas más externas, pero un átomo es más estable cuando se llenan todas las posiciones de electrones en la capa más externa. Debido a estas vacantes en las capas más externas, vemos la formación de enlaces químicos o interacciones entre dos o más elementos iguales o diferentes que resultan en la formación de moléculas. Para lograr una mayor estabilidad, los átomos tenderán a llenar completamente sus capas externas y se unirán con otros elementos para lograr este objetivo al compartir electrones, aceptando electrones de otro átomo o donando electrones a otro átomo. Debido a que las capas más externas de los elementos con números atómicos bajos (hasta calcio, con número atómico 20) pueden contener ocho electrones, esto se conoce como la regla del octeto. Un elemento puede donar o aceptar,
Cuando un átomo no contiene el mismo número de protones y electrones, se llama ion. Debido a que el número de electrones no es igual al número de protones, cada ion tiene una carga neta. Los iones positivos se forman al perder electrones y se denominan cationes. Los iones negativos se forman al ganar electrones y se denominan aniones.
Por ejemplo, el sodio solo tiene un electrón en su capa más externa. Se necesita menos energía para que el sodio done ese electrón que para aceptar siete electrones más para llenar la capa externa. Si el sodio pierde un electrón, ahora tiene 11 protones y solo 10 electrones, dejándolo con una carga general de +1. Ahora se llama ion de sodio.
El átomo de cloro tiene siete electrones en su capa externa. Una vez más, es más eficiente energéticamente que el cloro gane un electrón que pierda siete. Por lo tanto, tiende a ganar un electrón para crear un ion con 17 protones y 18 electrones, lo que le da una carga neta negativa (–1). Ahora se llama ión cloruro. Este movimiento de electrones de un elemento a otro se conoce como transferencia de electrones.
Enlaces iónicos
Hay cuatro tipos de enlaces o interacciones: iones, covalentes, enlaces de hidrógeno e interacciones de van der Waals. Los enlaces iónicos y covalentes son interacciones fuertes que requieren una mayor entrada de energía para separarse. Cuando un elemento dona un electrón de su capa externa, como en el ejemplo del átomo de sodio anterior, se forma un ion positivo. El elemento que acepta el electrón ahora está cargado negativamente. Debido a que las cargas positivas y negativas se atraen, estos iones permanecen juntos y forman un enlace iónico, o un enlace entre iones. Los elementos se unen con el electrón de un elemento que permanece predominantemente con el otro elemento. Cuando Na + y Cl – los iones se combinan para producir NaCl, un electrón de un átomo de sodio se queda con los otros siete del átomo de cloro, y los iones de sodio y cloruro se atraen entre sí en una red de iones con una carga neta cero.

Enlaces covalentes
Otro tipo de enlace químico fuerte entre dos o más átomos es un enlace covalente. Estos enlaces se forman cuando un electrón se comparte entre dos elementos y son la forma más fuerte y más común de enlace químico en los organismos vivos. Se forman enlaces covalentes entre los elementos que forman las moléculas biológicas en nuestras células. A diferencia de los enlaces iónicos, los enlaces covalentes no se disocian en el agua.
Los átomos de hidrógeno y oxígeno que se combinan para formar moléculas de agua están unidos por enlaces covalentes. El electrón del átomo de hidrógeno divide su tiempo entre la capa externa del átomo de hidrógeno y la capa externa incompleta del átomo de oxígeno.
Para llenar completamente la capa exterior de un átomo de oxígeno, dos electrones de dos átomos de hidrógeno se necesitan, de ahí, el subíndice “2” en H 2 O. Los electrones son compartidos entre los átomos, dividiendo su tiempo entre ellos para “relleno” el exterior cáscara de cada uno. Este intercambio es un estado de energía más bajo para todos los átomos involucrados que si existieran sin sus capas exteriores llenas.
Hay dos tipos de enlaces covalentes: polares y no polares. Los enlaces covalentes no polares se forman entre dos átomos del mismo elemento o entre diferentes elementos que comparten los electrones por igual. Por ejemplo, un átomo de oxígeno puede unirse con otro átomo de oxígeno para llenar sus capas exteriores. Esta asociación no es polar porque los electrones se distribuirán por igual entre cada átomo de oxígeno. Se forman dos enlaces covalentes entre los dos átomos de oxígeno porque el oxígeno requiere dos electrones compartidos para llenar su capa más externa.
Los átomos de nitrógeno formarán tres enlaces covalentes (también llamados triples covalentes) entre dos átomos de nitrógeno porque cada átomo de nitrógeno necesita tres electrones para llenar su capa más externa. Otro ejemplo de un enlace covalente no polar se encuentra en el metano (CH 4) molécula. El átomo de carbono tiene cuatro electrones en su capa más externa y necesita cuatro más para llenarlo. Obtiene estos cuatro de cuatro átomos de hidrógeno, cada átomo proporciona uno. Todos estos elementos comparten los electrones por igual, creando cuatro enlaces covalentes no polares (Figura 3).
En un enlace covalente polar, los electrones compartidos por los átomos pasan más tiempo más cerca de un núcleo que del otro. Debido a la distribución desigual de electrones entre los diferentes núcleos, se desarrolla una carga ligeramente positiva (δ +) o ligeramente negativa (δ–). Los enlaces covalentes entre los átomos de hidrógeno y oxígeno en el agua son enlaces covalentes polares. Los electrones compartidos pasan más tiempo cerca del núcleo de oxígeno, dándole una pequeña carga negativa, que pasan cerca de los núcleos de hidrógeno, dándoles a estas moléculas una pequeña carga positiva.

Enlaces de hidrógeno
Los enlaces iónicos y covalentes son enlaces fuertes que requieren una energía considerable para romperse. Sin embargo, no todos los enlaces entre elementos son enlaces iónicos o covalentes. También se pueden formar enlaces más débiles. Estas son atracciones que ocurren entre cargas positivas y negativas que no requieren mucha energía para romperse. Dos enlaces débiles que ocurren con frecuencia son los enlaces de hidrógeno y las interacciones de van der Waals. Estos enlaces dan lugar a las propiedades únicas del agua y las estructuras únicas de ADN y proteínas.
Cuando se forman enlaces covalentes polares que contienen un átomo de hidrógeno, el átomo de hidrógeno en ese enlace tiene una carga ligeramente positiva. Esto se debe a que el electrón compartido es atraído más fuertemente hacia el otro elemento y lejos del núcleo de hidrógeno. Debido a que el átomo de hidrógeno es ligeramente positivo (δ +), se sentirá atraído por las cargas parciales negativas vecinas (δ–). Cuando esto sucede, se produce una interacción débil entre la carga δ + del átomo de hidrógeno de una molécula y la carga δ– de la otra molécula. Esta interacción se llama enlace de hidrógeno.
Este tipo de enlace es común. Por ejemplo, la naturaleza líquida del agua es causada por los enlaces de hidrógeno entre las moléculas de agua. Los enlaces de hidrógeno le dan al agua las propiedades únicas que sostienen la vida. Si no fuera por la unión de hidrógeno, el agua sería un gas en lugar de un líquido a temperatura ambiente.
Se pueden formar enlaces de hidrógeno entre diferentes moléculas y no siempre tienen que incluir una molécula de agua. Los átomos de hidrógeno en enlaces polares dentro de cualquier molécula pueden formar enlaces con otras moléculas adyacentes. Por ejemplo, los enlaces de hidrógeno mantienen unidas dos largas cadenas de ADN para dar a la molécula de ADN su característica estructura de doble cadena. Los enlaces de hidrógeno también son responsables de parte de la estructura tridimensional de las proteínas.
Interacciones de Van Der Waals
Al igual que los enlaces de hidrógeno, las interacciones de van der Waals son atracciones débiles o interacciones entre moléculas. Ocurren entre átomos polares, unidos covalentemente, en diferentes moléculas. Algunas de estas atracciones débiles son causadas por cargas parciales temporales formadas cuando los electrones se mueven alrededor de un núcleo. Estas interacciones débiles entre las moléculas son importantes en los sistemas biológicos.
Tipos y funciones de las biomoléculas
Hay cuatro clases principales de biomoléculas: carbohidratos, proteínas, ácidos nucleicos y lípidos. Cada uno de ellos se discute a continuación.
Carbohidratos
Los carbohidratos se definen químicamente como polihidroxialdehídos o cetonas o compuestos que los producen por hidrólisis. En términos simples, reconocemos los carbohidratos como azúcares o sustancias que tienen un sabor dulce. Se llaman colectivamente como sacáridos (griego: sakcharon = azúcar). Dependiendo del número de unidades de azúcar constitutivas obtenidas por hidrólisis, se clasifican como monosacáridos (1 unidad), oligosacáridos (2-10 unidades) y polisacáridos (más de 10 unidades).
Tienen múltiples funciones y son la fuente dietética de energía más abundante; son estructuralmente muy importantes para muchos organismos vivos, ya que forman un componente estructural principal, por ejemplo, la celulosa es una fibra estructural importante para las plantas.

Proteínas
Las proteínas son otra clase de biomoléculas indispensables que representan alrededor del 50% del peso seco celular. Las proteínas son polímeros de aminoácidos dispuestos en forma de cadenas de polipéptidos. La estructura de las proteínas se clasifica en primaria, secundaria, terciaria y cuaternaria en algunos casos. Estas estructuras se basan en el nivel de complejidad del plegamiento de una cadena de polipéptidos. Las proteínas juegan roles estructurales y dinámicos. La miosina es la proteína que permite el movimiento por contracción de los músculos. La mayoría de las enzimas son de naturaleza proteica.
Aprende sobre las enzimas:
Ácidos nucleicos
Los ácidos nucleicos se refieren al material genético encontrado en la célula que transporta toda la información hereditaria de los padres a la progenie. Hay dos tipos de ácidos nucleicos, a saber, el ácido desoxirribonucleico (ADN) y el ácido ribonucleico (ARN). La función principal del ácido nucleico es la transferencia de información genética y síntesis de proteínas mediante procesos conocidos como traducción y transcripción.
La unidad monomérica de los ácidos nucleicos se conoce como nucleótido y está compuesta por una base nitrogenada, azúcar pentosa y fosfato. Los nucleótidos están unidos por un enlace fosfodiéster 3 ‘y 5’. La base de nitrógeno unida al azúcar pentosa hace que el nucleótido sea distinto.
Hay 4 bases nitrogenadas principales en el ADN: adenina, guanina, citosina y timina. En el ARN, la timina se reemplaza por uracilo. La estructura del ADN se describe como una estructura de doble hélice o doble hélice que se forma mediante enlaces de hidrógeno entre las bases de dos cadenas de polinucleótidos antiparalelos. En general, la estructura del ADN se parece a una escalera torcida.
Más sobre el ADN:
Lípidos
Los lípidos son sustancias orgánicas que son insolubles en agua, solubles en solventes orgánicos, están relacionados con los ácidos grasos y son utilizados por la célula viva. Incluyen grasas, ceras, esteroles, vitaminas liposolubles, mono, di o triglicéridos, fosfolípidos, etc. A diferencia de los carbohidratos, proteínas y ácidos nucleicos, los lípidos no son moléculas poliméricas. Los lípidos juegan un gran papel en la estructura celular y son la principal fuente de energía.
Compuestos orgánicos de seres vivos

Tal y como acabamos de ver, los seres vivos están compuestos de sólo cuatro clases de compuestos orgánicos: proteínas, carbohidratos, ácidos nucleicos y lípidos.
Estos compuestos son los compuestos de carbono. El átomo de carbono es vital en la molécula, ya que en ella forma la cadena básica a la que el resto de elementos químicos están unidos.
Los seres vivos disponen de compuestos orgánico. Éstos caracterizan a la materia viva y son la razón de las funciones que lleva a cabo. La diversidad de compuestos orgánicos que constituyen los seres vivos no son clasificados desde un sentido químico, sino por la solubilidad en agua. Se clasifican en:
- Glúcidos o hidratos de carbono y lípidos: sus funciones son estructurales y energéticas.
- Prótidos: son estructurales y enzimáticas.
- Ácidos nucleicos: son los responsables de la información genética.
Algunas sustancias son de gran importancia para los seres vivos pero estos las necesitan en muy pequeña cantidad y nunca tienen funciones energéticas ni estructurales. Por esta causa reciben el nombre de biocatalizadores. Son biocatalizadores las vitaminas, las enzimas y las hormonas.
Características del átomo de carbono

De la tabla periódica el carbono es el elemento número 6. Es el elemento más importante en los seres vivos, aunque no sea el más abundante. Podemos encontrarlo en la atmósfera en estado de CO₂, diluido en aguas constituyendo carbonatos. En la corteza se encuentra en las rocas calizas.
El átomo de carbono dispone de cuatro electrones en su última capa. Con ello consigue unirse a otros átomos por medio de cuatro enlaces covalentes.
El hidrógeno dispone de un electrón de valencia, con lo cual sólo podrá crear un enlace simple.
El oxígeno dispone de dos electrones de valencia, éste podrá crear dos enlaces simples o uno que puede ser doble.
El nitrógeno tiene tres electrones, con lo cual puede crear tres enlaces simples, uno doble o uno triple y otro simple.
Formación de las Biomoléculas

Las sustancias orgánicas se pueden representar por medio de distintos tipos de fórmulas:
Fórmulas desarrolladas o estructurales: En estas se especifican todos los átomos que componen la molécula y enlaces que los une. Estas fórmulas ofrecen mucha información, aunque las moléculas que son complejas es muy laborioso representarlas.
Las fórmulas semidesarrolladas: Éstas solo indican los enlaces de la cadena carbonada. Los demás átomos que se hayan juntos a un carbón concreto, se agrupan bajo ciertas normas.
Fórmulas empíricas: Éstas solo indican la cantidad de átomos de cada elemento que se encuentran en la molécula.
Cabe destacar que estas últimas fórmulas no ofrecen una idea de la estructura molecular. Pueden existir compuestos que, aunque sean distintos, pueden tener la misma fórmula empírica y distinta fórmula estructural.
En algunos casos, si la molécula es demasiado compleja, se puede recurrir a ciertas simplificaciones. De esta manera, las extensas cadenas carbonadas de ácidos grasos o de otras moléculas, se pueden representar bajo una línea quebrada en donde no se indican ni carbonos ni hidrógenos.

Sin embargo, sí que se indican las distintas funciones, los dobles enlaces u cualquier variación que tenga la molécula. También se facilitan las cadenas cíclicas, en donde a menudo tampoco se señalan ni los carbonos ni los hidrógenos.
Los esqueletos de las moléculas
Las distintas biomoléculas van a estar formadas por átomos de carbono juntos entre sí por medio de los enlaces covalentes. La resistencia y su versatilidad de enlaces como carbono-carbono y el carbono junto con otros elementos, como con el oxígeno, nitrógeno o azufre, posibilitarán que se puedan constituir estructuras que pasarán a ser el esqueleto de las principales moléculas.
También te puede interesar: